I. Hóa trị
- Hóa trị của một nguyên tố trong hợp chất là con số biểu thị khả năng liên kết của nguyên tử nguyên tố đó với nguyên tử khác trong phân tử.
- Hóa trị được biểu thị bằng các chữ số La Mã (I; II …)
- Để xác định hóa trị của nguyên tố trong hợp chất cộng hóa trị, người ta dựa vào hóa trị của nguyên tố đã biết làm đơn vị, chẳng hạn hóa trị của H là I; hóa trị của O là II.
Ví dụ:
Trong phân tử carbon dioxide (CO2) một nguyên tử C có khả năng liên kết với 2 nguyên tử O, mỗi nguyên tử O hóa trị II ⇒ C có hóa trị IV.
II. Quy tắc hóa trị
- Hóa trị và nguyên tử của các nguyên tố trong một số hợp chất tuân theo một quy tắc nhất định, gọi là quy tắc hóa trị.
- Quy tắc hóa trị: Trong phân tử hợp chất hai nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia.
- Ví dụ: Trong phân tử nước, hóa trị và số nguyên tử tham gia liên kết của H và O như sau:
Nguyên tố | H | O |
Hóa trị | I | II |
Số nguyên tử | 2 | 1 |
Tích hóa trị và số nguyên tử | I × 1 = II × 1 | |
III. Công thức hóa học
Phân tử của chất được tạo thành từ nguyên tử của một hay nhiều nguyên tố và được biểu diễn bằng công thức hóa học.
1. Viết công thức hóa học của đơn chất
- Công thức hóa học của đơn chất được kí hiệu bằng kí hiệu nguyên tố hóa học kèm với chỉ số (chỉ số nguyên tử của mỗi nguyên tố trong một phân tử) ghi ở bên dưới.
- Một số đơn chất phi kim thể khí (ở điều kiện thường) có công thức hóa học chung là Ax.
Ví dụ: Phân tử khí hydrogen được tạo thành từ hai nguyên tử hydrogen liên kết với nhau, công thức phân tử của khí hydrogen là H2.
- Đối với đơn chất kim loại, hạt hợp thành là nguyên tử nên kí hiệu hóa học của nguyên tố kim loại được coi là công thức hóa học của đơn chất kim loại.
Ví dụ: Kim loại sodium có công thức hóa học là Na.
- Một số đơn chất phi kim ở thể rắn, quy ước công thức hóa học là kí hiệu nguyên tố.
Ví dụ: Công thức hóa học của đơn chất carbon là C.
2. Viết công thức hóa học của hợp chất
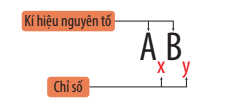
- Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo thành kèm chỉ số ở bên dưới mỗi kí hiệu.
- Công thức chung của phân tử có dạng: AxBy
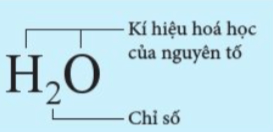
Ví dụ: Công thức hóa học của nước là H2O
- Công thức hóa học cho biết thành phần nguyên tố và số lượng nguyên tử của mỗi nguyên tố có trong phân tử đó. Từ đó, có thể tính được khối lượng phân tử.
Chú ý: Cách viết công thức hóa học hợp chất
- Hợp chất tạo bởi oxygen và nguyên tố khác, công thức hóa học có dạng AxOy.
- Nếu A là kim loại và B là phi kim, công thức hóa học có dạng AxBy.
- Hợp chất tạo bởi hydrogen và nguyên tố A:
+ Nếu A thuộc các nhóm IA đến VA, công thức hóa học có dạng AHx.
+ Nếu A thuộc các nhóm VIA đến VIIA, công thức hóa học có dạng HxA.
IV. Tính phần trăm nguyên tố trong hợp chất
- Phần trăm (%) nguyên tố trong hợp chất được tính bằng tỉ số giữa khối lượng của nguyên tố đó trong một phân tử hợp chất và khối lượng phân tử (KLPT) của hợp chất.
- Khối lượng của nguyên tố trong một phân tử hợp chất được tính bằng tích của khối lượng nguyên tử (KLNT) và số nguyên tử của nguyên tố đó.
- Tổng quát:
+ Với hợp chất AxBy, ta có:
+ Tổng tất cả các phần trăm nguyên tố trong một phân tử luôn bằng 100%.
- Ví dụ: Đối với hợp chất Al2O3
%O = 100% - 52,94% = 47,06%
V. Xác định công thức hóa học
1. Xác định công thức hóa học khi biết phần trăm nguyên tố và khối lượng phân tử:
- Các bước xác định:
Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát);
Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất;
Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm.
- Ví dụ minh họa:
Phân tử X có 75% khối lượng là aluminium, còn lại là carbon. Xác định công thức phân tử của X, biết khối lượng phân tử của nó là 144 amu.
Hướng dẫn giải:
%C = 100% - %Al = 100% - 75% = 25%
⇒ x = 4
⇒ y = 3
Vậy công thức hóa học của hợp chất là Al4C3
2. Xác định công thức hóa học dựa vào quy tắc hóa trị
- Các bước xác định:
+ Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát)
+ Bước 2: Lập biểu thức tính dựa vào quy tắc hóa trị, chuyển thành tỉ lệ các chỉ số nguyên tử.
+ Bước 3: Xác định số nguyên tử (những số nguyên đơn giản nhất, có tỉ lệ tối giản) và viết công thức hóa học cần tìm.
- Ví dụ: Hợp chất tạo bởi oxygen và potassium có dạng:
Theo quy tắc hóa trị ta có: x × I = y × II
Chuyển thành tỉ lệ:
Chọn x = 2; y = 1
Vậy công thức hóa học của hợp chất là K2O
Chú ý:
- Quy tắc hóa trị thường đúng với đa số hợp chất vô cơ. Tuy nhiên, quy tắc này không đúng với đa số hợp chất hữu cơ (C2H4; C6H6 …) và một số hợp chất vô cơ (H2O2; Na2O2 …)
BÀI VIẾT LIÊN QUAN (Giải SGK)
Chủ đề 1. Nguyên tử - Nguyên tố hóa học - Sơ lược về bảng tuần hoàn các nguyên tố hóa học
3. Bài 4. Sơ lược bảng tuần hoàn các nguyên tố hóa học
Chủ đề 2. Phân tử
1. Bài 5. Phân tử - Đơn chất - Hợp chất
2. Bài 6. Giới thiệu về liên kết hóa học
3. Bài 7. Hóa trị và công thức hóa học
Chủ đề 1. Nguyên tử - Nguyên tố hóa học - Sơ lược về bảng tuần hoàn các nguyên tố hóa học
3. Bài 4. Sơ lược bảng tuần hoàn các nguyên tố hóa học
Chủ đề 2. Phân tử
1. Bài 5. Phân tử - Đơn chất - Hợp chất
2. Bài 6. Giới thiệu về liên kết hóa học
3. Bài 7. Hóa trị và công thức hóa học
Đọc thêm:
Câu hỏi :
Viết công thức hóa học các hợp chất tạo bởi oxygen và mỗi nguyên tố sau: potassium, magnesium, aluminium, phosphorus (hóa trị V)
Viết công thức hóa học các hợp chất tạo bởi oxygen và mỗi nguyên tố sau: potassium, magnesium, aluminium, phosphorus (hóa trị V)
* Đáp án
* Hướng dẫn giải
- Hợp chất tạo bởi oxygen và potassium có dạng:
Theo quy tắc hóa trị ta có: x × I = y × II
Chuyển thành tỉ lệ:
Chọn x = 2; y = 1
Vậy công thức hóa học của hợp chất là K2O
- Hợp chất tạo bởi oxygen và magnesium có dạng:
Theo quy tắc hóa trị ta có: x × II = y × II
Chuyển thành tỉ lệ:
Chọn x = 1; y = 1
Vậy công thức hóa học của hợp chất là MgO
- Hợp chất tạo bởi oxygen và aluminium có dạng:
Theo quy tắc hóa trị ta có: x × III = y × II
Chuyển thành tỉ lệ:
Chọn x = 2; y = 3
Vậy công thức hóa học của hợp chất là Al2O3
- Hợp chất tạo bởi oxygen và phosphorus có dạng:
Theo quy tắc hóa trị ta có: x × V = y × II
Chuyển thành tỉ lệ:
Chọn x = 2; y = 5
Vậy công thức hóa học của hợp chất là P2O5

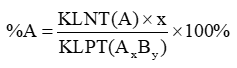
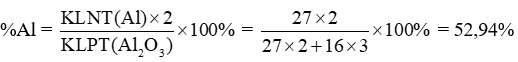
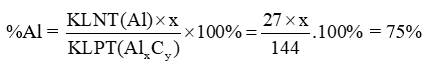
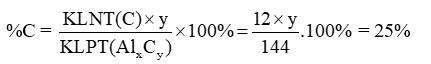
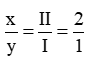
0 Comments:
Đăng nhận xét