A. Lý thuyết & Phương pháp giải
- Khối lượng của các hạt cấu tạo nên nguyên tử:
+ Khối lượng của một electron: me = 9,1094.10-31 kg.
+ Khối lượng của một proton: mp = 1,6726.10-27 kg.
+ Khối lượng của một nơtron: mn = 1,6748.10-27 kg.
Nhận xét: Proton và nơtron có khối lượng xấp xỉ nhau và chúng lớn hơn khối lượng của electron khoảng 1836 lần, do đó có thể coi khối lượng của nguyên tử tập trung chủ yếu ở hạt nhân nguyên tử (khối lượng của các electron là không đáng kể, có thể bỏ qua).
- Nguyên tử có khối lượng vô cùng nhỏ bé, nếu tính bằng đơn vị gam thì số trị quá bé, không tiện sử dụng. Do đó, quy ước lấy 1/12 khối lượng của nguyên tử C làm đơn vị khối lượng cho nguyên tử, gọi là đơn vị cacbon, viết tắt là đvC, kí hiệu quốc tế là u.
Chú ý:
+) Khối lượng tính bằng đơn vị cacbon chỉ là khối lượng tương đối giữa các nguyên tử. Người ta gọi khối lượng này là nguyên tử khối.
Nguyên tử khối là khối lượng của một nguyên tử tính theo đơn vị cacbon.
Ví dụ: nguyên tử khối của cacbon là 12 đvC, nguyên tử khối của H là 1đvC,…
1 đvC = 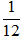
⇒ 1 đvC = 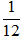
Vậy mp ≈ mn ≈ 1u; me ≈ 0,00055u.
+) Nguyên tử hiđro có khối lượng nhẹ nhất.
- Khối lượng nguyên tử được tính bằng tổng khối lượng các hạt trong nguyên tử:
mnguyên tử = ∑mp + ∑mn + ∑me
- Do khối lượng electron quá nhỏ bé so với khối lượng của proton và nơtron nên khối lượng nguyên tử được tính xấp xỉ bằng:
mnguyên tử = ∑mp +∑mn = mhạt nhân
- Đơn vị khối lượng nguyên tử là u.
1u = 1,6605.10-27 kg = 1,6605.10-24 g.
Lưu ý:
+ mp = mn = 1u; me = 0,00055u.
+) Nguyên tử khối của một số nguyên tố hay gặp (trang 42 – SGK hóa học 8).
| Số proton | Tên nguyên tố | Kí hiệu hóa học | Nguyên tử khối | Hóa trị |
| 1 | Hiđro | H | 1 | I |
| 2 | Heli | He | 4 | |
| 3 | Liti | Li | 7 | I |
| 4 | Beri | Be | 9 | II |
| 5 | Bo | B | 11 | 11 III |
| 6 | Cacbon | C | 12 | IV, II |
| 7 | Nitơ | N | 14 | III, II, IV… |
| 8 | Oxi | O | 16 | II |
| 9 | Flo | F | 19 | I |
| 10 | Neon | Ne | 20 | |
| 11 | Natri | Na | 23 | I |
| 12 | Magie | Mg | 24 | II |
| 13 | Nhôm | Al | 27 | III |
| 14 | Silic | Si | 28 | IV |
| 15 | Photpho | P | 31 | III, V |
| 16 | Lưu huỳnh | S | 32 | II, IV,VI |
| 17 | Clo | Cl | 35,5 | I, … |
| 18 | Agon | Ar | 39,9 | |
| 19 | Kali | K | 39 | I |
| 20 | Canxi | Ca | 40 | II |
| . | ||||
| . | ||||
| . | ||||
| 24 | Crom | Cr | 52 | II, III, … |
| 25 | Mangan | Mn | 55 | II, IV, VII… |
| 26 | Sắt | Fe | 56 | II, III |
| 29 | Đồng | Cu | 64 | I, II |
| 30 | Kẽm | Zn | 65 | II |
| 35 | Brom | Br | 80 | I, … |
| 47 | Bạc | Ag | 108 | I |
| 56 | Bari | Ba | 137 | II |
| 80 | Thủy ngân | Hg | 201 | I, II |
| 82 | Chì | Pb | 207 | II, IV |
B. Ví dụ minh họa
Ví dụ 1: Biết nguyên tử nhôm có 13 proton, 14 nơtron. Khối lượng tính bằng gam của một nguyên tử nhôm là
A. 5,32.10-23g.
B. 6,02.10-23g.
C. 4,48.10-23g.
D. 3,99.10-23g.
Lời giải:
Chọn C
mAl ≈ ∑mp + ∑mn = 13u + 14u = 27u.
Có 1u = 1,6605.10-27kg ⇒ mAl = 27. 1,6605.10-27.1000 = 4,48.10-27g.
Ví dụ 2: Hãy so sánh xem nguyên tử magie nặng hay nhẹ hơn bao nhiêu lần so với nguyên tử cacbon?
Lời giải:
Nguyên tử khối của Mg là 24 đvC; nguyên tử khối của cacbon là 12 đvC.
⇒Nguyên tử magie nặng hơn 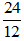
Ví dụ 3: Nguyên tử X nặng gấp 4 lần nguyên tử nitơ. Tính nguyên tử khối của X và cho biết X thuộc nguyên tố nào?
Lời giải:
Nguyên tử khối của nitơ = 14 đvC
⇒ Nguyên tử khối của X = 4 x 14 = 56 (đvC)
Vậy X là nguyên tố sắt (Fe).
Ví dụ 4: Cho biết 1u = 1,6605.10-27 kg, nguyên tử khối của oxi bằng 15,999u. Hãy tính khối lượng của một nguyên tử oxi bằng bao nhiêu kg?
A. 2,6566.10-26 kg.
B. 3,2045.10-26 kg.
C. 1,6809.10-26 kg.
D. 4,0237.10-26 kg.
Hướng dẫn giải:
Lời giải
Đáp án A
mO = 15,999 . 1,6605.10-27 = 2,6566.10-26 kg.
Ví dụ 5: Cho nguyên tử Na có 11 electron, 11proton, 12 nơtron. Hãy tính khối lượng của nguyên tử trên ra đơn vị kg?
A. 342,6005.10-28 kg.
B. 385,0622.10-28 kg.
C. 295,9807.10-28 kg.
D. 402,0267.10-28 kg.
Hướng dẫn giải:
Lời giải
Đáp án B
mNa = mp + mn + me
= 11 . 1,6726.10-27 + 12 . 1,6748.10-27 + 11 . 9,1094.10-31
= 385,0622.10-28 kg.
C. Bài tập vận dụng
Câu 1: Nguyên tử khối là
A. Khối lượng của nguyên tử tính bằng gam.
B. Khối lượng của phân tử tính bằng đvC.
C. Khối lượng của nguyên tử tính bằng đvC.
D. Khối lượng của phân tử tính bằng gam.
Lời giải:
Chọn C.
Câu 2: Nguyên tử khối của clo là
A. 71 đvC.
B. 35,5 gam.
C. 71 gam.
D. 35,5 đvC.
Lời giải:
Chọn D.
Câu 3: Khối lượng của một nguyên tử cacbon là 19,9265. 10-23 gam. Vậy ta có khối lượng của 1 đvC là
A. 8,553. 10-23 g.
B. 2,6605. 10-23 g.
C. 0,16605. 10-23 g.
D. 18,56. 10-23 g.
Lời giải:
Chọn C.
⇒ 1 đvC = 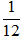
Câu 4: Biết rằng bốn nguyên tử Mg nặng bằng ba nguyên tử của nguyên tố X. Vậy tên của nguyên tố X là
A. Lưu huỳnh.
B. Sắt.
C. Nitơ.
D. Can xi.
Lời giải:
Chọn A
Nguyên tử khối của Mg là 24 đvC. Đặt nguyên tử khối của X là M.
Theo bài ra, ta có: 4.24 = 3.M ⇒ M = 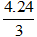
Vậy X là nguyên tố lưu huỳnh (S).
Câu 5: Khối lượng tương đối của một phân tử H2O là
A. 18 đvC.
B. 18 gam.
C.34 đvC.
D. 18kg.
Lời giải:
Chọn A.
Khối lượng tương đối của một phân tử nước = MH2O = 2.1 + 16 = 18 (đvC).
Câu 6: Biết nguyên tử nitơ gồm có 7 proton, 7 nơtron và 7 electron. Khối lượng của toàn nguyên tử nitơ là
A. 14 gam.
B. 21 gam.
C. 2,34. 10-23 gam.
D. 2,34. 10-27 gam.
Lời giải:
Chọn C.
Ta có:
mC = ∑mp + ∑me + ∑mn = 7. 1,6726.10-27 + 7. 9,1094.10-31 + 7.1,6748.10-27
= 2,34.10-26kg = 2,34.10-23 gam.
Câu 7: Trường hợp nào đưới đây có sự tương ứng giữa hạt cơ bản với khối lượng và điện tích của chúng?
A. proton, m = 0,00055u, q = 1+.
B. nơtron, m = 1,0086u, q = 0.
C. electron, m = 1,0073u, q =1-.
D. proton, m = 1,0073u, q = 1-.
Lời giải:
Chọn B.
A sai vì mp ≈ 1u.
C sai vì me ≈ 0,00055u.
D sai vì proton mang điện tích dương.
Câu 8: Một nguyên tử chỉ có 1 electron ở vỏ nguyên tử. Hạt nhân nguyên tử có khối lượng xấp xỉ 3u. Số hạt proton và hạt nơtron trong hạt nhân nguyên tử này lần lượt là
A. 1 và 0.
B. 1 và 2.
C. 1 và 3.
D. 3 và 0.
Lời giải:
Chọn B.
Ta có: mP ≈ mn ≈ 1u
Tổng số hạt n và p trong hạt nhân nguyên tử này là: 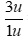
Nguyên tử có 1 electron ở lớp vỏ nguyên tử nên sẽ có 1 proton trong hạt nhân. Suy ra số hạt nơtron trong hạt nhân là 2.
Câu 9: Hai nguyên tử Mg nặng gấp mấy lần nguyên tử O?
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Chọn C.
Khối lượng của 2 nguyên tử Mg là 2.24 = 48đvC.
Khối lượng của nguyên tử O là 16 đvC.
Tỉ lệ khối lượng của 2 nguyên tử Mg so với nguyên tử O là: 48 : 16 = 3 lần.
Vậy 2 nguyên tử magie nặng bằng 3 nguyên tử oxi.
Câu 10: Tỉ số về khối lượng của electron so với proton là
A. 1836.
B. 5,4463.
C. 5,4463.10-4.
D. 0,055.
Lời giải:
Chọn C.
Tỉ số về khối lượng của electron so với proton là:
D. Bài tập tự luyện
Câu 1: Nguyên tố X có nguyên tử khối bằng 3,5 lần nguyên tử khối của oxygen. X là nguyên tố nào sau đây?
A. Ca.
B. Na.
C. K.
D. Fe.
Câu 2: Một nguyên tử chỉ có 1 electron ở vỏ nguyên tử. Hạt nhân nguyên tử có khối lượng xấp xỉ 3 amu. Số hạt proton và hạt neutron trong hạt nhân nguyên tử này lần lượt là
A. 1 và 0.
B. 1 và 2.
C. 1 và 3.
D. 3 và 0.
Câu 3: Biết rằng 4 nguyên tử N nặng bằng nguyên tử của nguyên tố X. Vậy tên của nguyên tố X là
A. Calcium.
B. Sắt.
C. Nitrogen.
D. Oxygen.
Câu 4: Biết nguyên tử sodium có 11 proton, 12 neutron. Khối lượng tính bằng gam của một nguyên tử sodium là bao nhiêu?
Câu 5: Hãy so sánh xem:
a) Nguyên tử lưu huỳnh nặng hay nhẹ hơn, bằng bao nhiêu lần so với nguyên tử đồng.
b) Nguyên tử silicon nặng hay nhẹ hơn, bằng bao nhiêu lần so với nguyên tử sắt.
Câu 6: Khối lượng của một nguyên tử oxi là bao nhiêu đvC?
A. 8 đvC.
B. 16 đvC.
C. 20 đvC.
D. 24 đvC.
Hướng dẫn giải:
Lời giải
Đáp án B.
Câu 7: Để biểu thị khối lượng của một nguyên tử, người ta dùng đơn vị nào?
A. gam.
B. miligam.
C. kilogam.
D. đvC.
Hướng dẫn giải:
Lời giải
Đáp án D.
Câu 8: Nguyên tử Y nặng gấp 2 lần nguyên tử lưu huỳnh. Hãy cho biết Y là nguyên tố nào?
A. Ca.
B. Na
C. Cu.
D. Zn.
Hướng dẫn giải:
Lời giải
Đáp án C
Câu 9: Nguyên tử Al có 13 electron, 13 proton, 14 nơtron. Tính khối lượng của nguyên tử trên theo đơn vị u?
A. 25,12067u.
B.26.11209u.
C. 28,10238u.
D. 27,00715u.
Hướng dẫn giải:
Lời giải
Đáp án D.
mAl = 13u + 14u + 13.0,00055u
= 27,00715u.
Câu 10: Nguyên tử lưu huỳnh nặng gấp mấy lần nguyên tử hidro?
A. 16 lần.
B. 32 lần.
C.20 lần.
D. 25 lần.
Hướng dẫn giải:
Lời giải
Đáp án B.
Câu 11: Hãy cho biết mối liên hệ giữa số proton và số đơn vị điện tích hạt nhân là
A. Số proton bằng số đơn vị điện tích hạt nhân.
B. Số proton lớn hơn số đơn vị điện tích hạt nhân.
C. Số proton nhỏ hơn số đơn vị điện tích hạt nhân.
D. Số proton khác số đơn vị điện tích hạt nhân.
Hướng dẫn giải:
Lời giải
Đáp án A.
Câu 12: Tìm tỉ số về khối lượng của electron với proton?
A. 4,2367.10-4.
B. 5,4463.10-4.
C. 6,4325.10-4.
D. 3,2879.10-4.
Lời giải
Đáp án B.
Câu 13: Khối lượng của một nguyên tử cacbon-12 là bao nhiêu?
A. 12u.
B. 12 gam.
C. 1 đvC.
D. 1u
Hướng dẫn giải:
Lời giải
Đáp án A.
Câu 14: Cho nguyên tử Na có 11electron, 11 proton, 12 nơtron. Tính khối lượng của
1024 nguyên tử Na ra đơn vị gam?
A. 36,2018g.
B. 39,2102g.
C. 38,2015g.
D. 34,2019g.
Hướng dẫn giải:
Lời giải
Đáp án C.
Ta có: mNa = 11u + 12u + 11.0,00055u = 23,00605u
Khối lượng của 1024 nguyên tử Na là: 1024 . 23,00605 . 1,6605.10-24 = 38,2015 g.
Câu 15: Vì sao khối lượng nguyên tử được coi bằng khối lượng hạt nhân. Chọn đáp án đúng.
A. Do proton và nơtron có cùng khối lượng còn electron có khối lượng rất bé.
B. Do số p = số e.
C. Do hạt nhân tạo bởi proton và nơtron.
D. Do nơtron không mang điện.
Hướng dẫn giải:
Lời giải
Đáp án A.

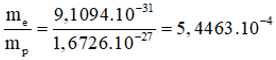
0 Comments:
Đăng nhận xét