Một số kiến thức cần nắm vững về muối:
1. Khái niệm
- Phân tử muối gồm có một hay nhiều nguyên tử kim loại liên kết với một hay nhiều gốc axit.
- Ví dụ: NaCl, CuSO4, CaCO3, NaNO3,...
2. Công thức hóa học
- Thành phần phân tử: một hay nhiều nguyên tử kim loại và một hay nhiều gốc axit.
- Công thức hóa học dạng: MxAy
Trong đó:
- M : là nguyên tử kim loại.
- A : là gốc axit.
Ví dụ: Na2CO3 NaHCO3
Gốc axit : =CO3 - HCO3
3. Tên gọi
- Tên muối = Tên KL + hoá trị (nếu KL có nhiều hoá trị) + tên gốc axit
Ví dụ:
Na2SO4: Natri sunfat
Na2SO3: Natri sunfit
- Tên gốc axit:
+ Gốc axit tương ứng với axit không có oxi: Tên gốc = tên phi kim + ua
+ Gốc axit tương ứng với axit có nhiều oxi: Tên gốc = tên phi kim + at
+ Gốc axit tương ứng với axit có ít oxi: Tên gốc = tên phi kim + it
Xác định công thức hoá học của muối khi biết thành phần các nguyên tố
Gọi công thức tổng quát của hợp chất là AxBy
Bước 1: Tìm khối lượng mỗi nguyên tố có trong 1 mol hợp chất.
mA = 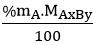
Bước 2: Tìm số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất.
Bước 3: Lập công thức hóa học của hợp chất.
B. Ví dụ minh họa
Ví dụ 1: Viết công thức hóa học của những muối có tên gọi sau: Sắt (III) sunfat, Magie hiđrocacbonat, Kẽm sunfat, Đồng (II) clorua
Lời giải:
Sắt (III) sunfat: Fe2(SO4)3
Magie hiđrocacbonat: Mg(HCO3)2
Kẽm sunfat: ZnSO4
Đồng (II) clorua: CuCl2
Ví dụ 2: Cho các sơ đồ phản ứng sau:
NaOH + HCl → NaCl + H2O
Al(OH)3+ H2SO4 → Al2(SO4) + H2O
a) Lập phương trình hóa học của phản ứng có sơ đồ trên
b) Gọi tên các muối tạo thành
Lời giải:
a) Phương trình hóa học:
NaOH + HCl → NaCl + H2O
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
b) Gọi tên các muối tạo thành:
NaCl: Natri clorua
Al2(SO4)3: Nhôm sunfat
Ví dụ 3: Muối A chứa Ca, C và O. Biết thành phần phần trăm về khối lượng của các nguyên tố Ca, C, O lần lượt là: 40%, 12%, 48%. Xác định công thức hóa học của A biết khối lượng mol của hợp chất là: 100 g/mol
Lời giải:
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCa = 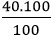
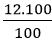
mO = 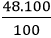
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất là:
nCa = 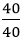
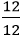
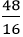
Vậy công thức hoá học của hợp chất là: CaCO3 (Canxi cacbonat)
C. Bài tập vận dụng
Câu 1: Công thức hóa học của muối bạc clorua là:
A. AgCl2
B. Ag2Cl
C. Ag2Cl3
D. AgCl
Lời giải:
Đáp án D
Tên muối = Tên KL (kèm theo hoá trị nếu KL có nhiều hoá trị) + tên gốc axit
⇒ Công thức hóa học của bạc clorua là AgCl
Câu 2: Công thức hóa học của muối nhôm clorua là:
A. AlCl.
B. Al3Cl.
C. AlCl3.
D. Al3Cl2.
Lời giải:
Đáp án C
Tên muối = Tên KL (kèm theo hoá trị nếu KL có nhiều hoá trị) + tên gốc axit
⇒ Công thức hóa học của muối nhôm clorua là AlCl3
Câu 3: Hợp chất Na2SO4 có tên gọi là:
A. natri sunfat.
B. natri sunfit.
C. sunfat natri.
b. natri sunfuric.
Lời giải:
Đáp án A
Tên muối = Tên KL (kèm theo hoá trị nếu KL có nhiều hoá trị) + tên gốc axit
⇒ tên gọi của Na2SO4 là: Natri sunfat
Câu 4: Hợp chất nào sau đây không phải là muối?
A. Đồng (II) nitrat
B. Kali clorua
C. Sắt (II) sunfat
D. Canxi hiđroxit
Lời giải:
Đáp án D
Muối = kim loại + gốc axit
Hợp chất không phải muối là: Canxi hiđroxit vì canxi hiđroxit thuộc loại bazơ
Câu 5: Cho các chất sau: CaO, H2SO4, Fe(OH)2, FeSO4, CaSO4, HCl, LiOH, MnO2, CuCl2, Al(OH)3, SO2. Có bao nhiêu hợp chất là muối?
A. 3
B. 4
C. 5
D. 6
Lời giải:
Đáp án A
Phân tử muối gồm có một hay nhiều nguyên tử kim loại liên kết với một hay nhiều gốc axit ⇒ Các muối là: FeSO4, CaSO4, CuCl2
Câu 6: Cho phương trình sau: Zn +H2SO4 → ZnSO4 +H2↑. Tên gọi của muối thu được là:
A. Kẽm (II) sunfat
B. Kẽm sunfat
C. Kẽm (II) sunfit
D. Sunfat kẽm
Lời giải:
Đáp án B
Tên muối = Tên KL (kèm theo hoá trị nếu KL có nhiều hoá trị) + tên gốc axit
⇒ tên gọi của ZnSO4 là: Kẽm sunfat.
Câu 7: Dãy chất nào sau đây chỉ bao gồm muối:
A. MgCl2; Na2SO4; KNO3
B. Na2CO3; H2SO4; Ba(OH)2
C. CaSO4; HCl; MgCO3
D. H2O; Na3PO4; KOH
Lời giải:
Đáp án A
Dãy chất chỉ toàn bao gồm muối là: MgCl2; Na2SO4; KNO3
Loại B vì H2SO4 là axit, Ba(OH)2 là bazơ
Loại C vì HCl là axit
Loại D vì H2O không phải muối, KOH là bazơ
Câu 8: Một hợp chất gồm 2 nguyên tố kết hợp với nhau theo tỉ lệ khối lượng là 3 phần magie với 4 phần lưu huỳnh. Tìm công thức hóa học đơn giản của hợp chất đó?
A. MgS.
B. Mg2S.
C. MgS2.
D. Mg2S2
Lời giải:
Đáp án A
Giả sử phần Mg có khối lượng 3 gam → phần lưu huỳnh có khối lượng 4 gam.
Số mol Mg kết hợp với lưu huỳnh: nMg = 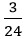
Số mol S kết hợp với magie: nS = 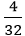
Vậy 0,125 mol nguyên tử Mg kết hợp với 0,125 mol nguyên tử S
Nên công thức hóa học đơn giản của hợp chất là MgS (Magie sunfua)
Câu 9: Một hơp chất có thành phần các nguyên tố là 40% Cu; 20% S và 40% O. Hãy xác định công thức hoá học của hợp chất (biết khối lượng mol của hợp chất là 160 g/mol)
A. CuSO3
B. CuSO4
C. Cu2SO4
D. Cu2(SO4)3
Lời giải:
Đáp án B
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất là:
Vậy công thức hoá học của hợp chất là: CuSO4
Câu 10: Hợp chất A có khối lượng mol 58,5 g/mol, thành phần phần trăm theo khối lượng của các nguyên tố là: 60,68% Cl, còn lại là Na. Công thức hóa học của hợp chất là:
A. NaCl
B. NaCl2
C. Na2Cl
D. Na2Cl2
Lời giải:
Đáp án A
Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCl = 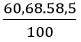
Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là:
nCl = 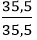
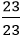
Vậy công thức hoá học của hợp chất là NaCl (Natri clorua)

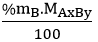
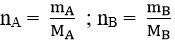
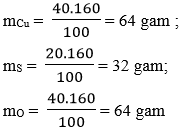
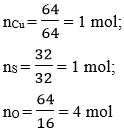
0 Comments:
Đăng nhận xét