I. Phản ứng hoá học
Quá trình biến đổi chất này thành chất khác được gọi là phản ứng hoá học.
Chất tham gia phản ứng gọi là chất đầu.
Chất mới tạo thành gọi là sản phẩm.
Ví dụ: Hỗn hợp sắt (iron) và lưu huỳnh (sulfur) đã phản ứng với nhau khi đun nóng để tạo thành hợp chất iron(II) sulfide (FeS).
Trong đó chất đầu là sắt và lưu huỳnh; sản phẩm là iron(II) sulfide.
II. Diễn biến của phản ứng hoá học
Trong phản ứng hoá học, có sự phá vỡ liên kết cũ và hình thành liên kết mới. Kết quả là chất này biến đổi thành chất khác.
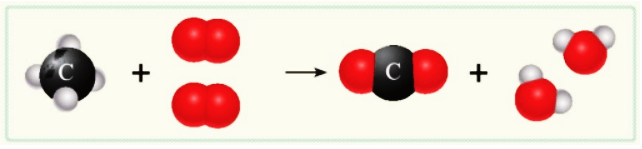
Sơ đồ mô tả phản ứng đốt cháy khí methane trong không khí
thu được carbon dioxide và nước
III. Một số dấu hiệu nhận biết có phản ứng hoá học xảy ra
Một số dấu hiệu có thể nhận biết phản ứng hoá học xảy ra: xuất hiện chất khí, chất kết tủa; thay đổi màu sắc, mùi; phát sáng, giải phóng hoặc hấp thụ nhiệt năng, …
 |  |
Gas cháy sẽ toả nhiệt | Phản ứng phân huỷ đường thành than và hơi nước |
 |  |
Kẽm tác dụng với dung dịch hydrochloric acid tạo bọt khí | Chất kết tủa tạo thành sau phản ứng |
IV. Năng lượng trong phản ứng hoá học
1. Phản ứng toả nhiệt, phản ứng thu nhiệt
Trong một phản ứng hoá học, luôn có sự thay đổi năng lượng. Năng lượng có thể tỏa ra hoặc nhận vào, thường dưới dạng nhiệt. Vì vậy, ta có thể chia phản ứng thành hai nhóm: phản ứng toả nhiệt và phản ứng thu nhiệt.
+ Phản ứng toả nhiệt là phản ứng có sự giải phóng năng lượng ra môi trường bên ngoài, thể hiện ở sự gia tăng nhiệt độ.
Những phản ứng toả nhiệt có thể được viết tổng quát như sau:
Chất phản ứng → Sản phẩm + năng lượng
+ Phản ứng thu nhiệt là những phản ứng hấp thụ năng lượng từ môi trường xung quanh.
Những phản ứng thu nhiệt có thể được viết tổng quát như sau:
Chất phản ứng + năng lượng → Sản phẩm
2. Các ứng dụng phổ biến của phản ứng toả nhiệt
Sự đốt cháy nhiên liệu (than, dầu hoả, gas, …) tạo ra năng lượng nhiệt phục vụ cho việc nấu nướng, sưởi ấm, …
Quá trình hô hấp trong cơ thể cung cấp năng lượng để cơ thể hoạt động, đồng thời tạo nên thân nhiệt ổn định và hỗ trợ quá trình vận động.

0 Comments:
Đăng nhận xét